近年来,基因转导通过病毒载体已成为操控神经元及其电路活动的研究重点。其中,重组腺相关病毒(AAV)载体在光遗传学和化学遗传学等尖端技术中得到广泛应用。虽然在向目标神经元群体进行基因转导方面取得了可观进展,但不同的AAV血清型表现出不同的感染特性。在灵长类动物和啮齿动物大脑的基因转导实验中,常用AAV1、AAV5和AAV9载体。然而,这些载体在对神经元和胶质细胞感染时,可能引发炎症反应。相比之下,AAV2表现出较高的神经元特异性,但其转基因表达能力较低。因此,需要一种在转基因表达和神经元特异性方面都具有优越性的AAV载体。
京都大学灵长类研究所和人类行为进化起源中心的研究者们开发了一种由AAV1和AAV2的外壳蛋白组成的镶嵌载体,名为AAV2.1载体,旨在实现同时的高转基因表达和神经元特异性。通过与原始AAV2和AAV1载体进行比较,研究分析了AAV2.1载体在猕猴前额皮层中的基因转导特性。此外,还探讨了AAV2.1载体在纹状体和视觉皮层中进行化学遗传学操作和体内钙成像方面的应用。研究成果以“A mosaic adeno-associated virus vector as a versatile tool that exhibits high levels of transgene expression and neuron specificity in primate brain”为题,发表在Nature Communications(IF:17.694)上。

研究 结果
1. 制备镶嵌式AAV载体
研究者们制备了两种不同比例的镶嵌式AAV载体其中包含不同比例的AAV1和AAV2外壳蛋白:AAV2.1-A载体,其外壳由10% AAV1外壳蛋白和90% AAV2外壳蛋白组成;以及AAV2.1-B载体,其外壳由50% AAV1外壳蛋白和50% AAV2外壳蛋白组成。根据之前的体外研究,最初制备了AAV2.1-B载体,但发现存在一定程度的胶质感染性。因此,随后制备了AAV2.1-A载体,其中AAV1外壳蛋白的比例降低到10%。在三组实验中使用了14种不同的载体,包括基因转导特性的形态学分析、神经元活动的化学遗传学调制,以及神经元活动的体内钙成像。结果显示,AAV2.1和AAV1载体的效率普遍高于AAV2载体。
2.镶嵌式AAV载体的基因转导特性
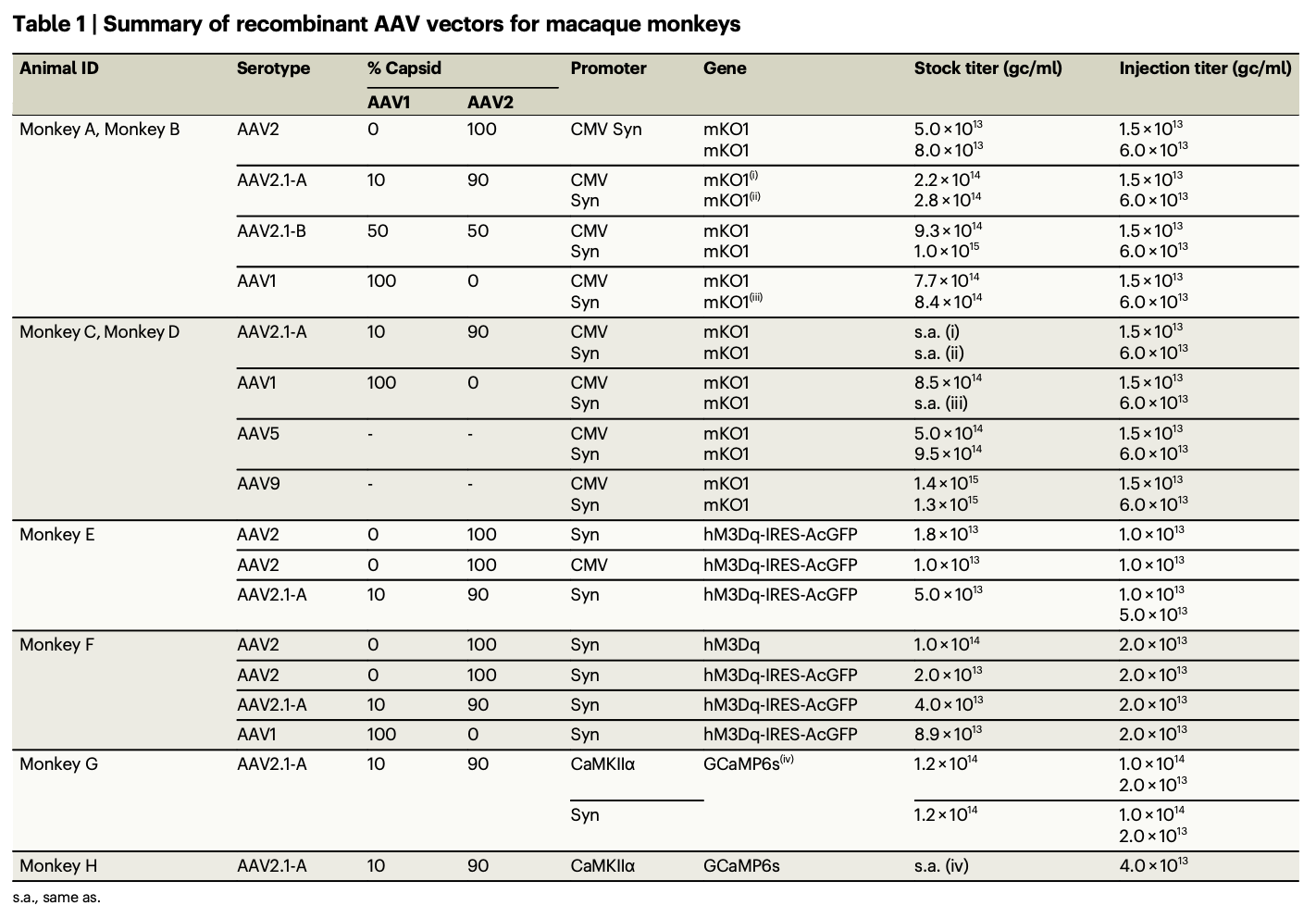
研究者首先通过将拼接式AAV2.1-A和AAV2.1-B载体与原始的AAV2和AAV1载体进行比较,探究了它们的基因转导特性。研究中使用了广泛表达的CMV启动子和神经元特异性的Syn启动子,分别评估了载体的神经元特异性和神经元内的转基因表达水平。在两只恒河猴的额叶中央壁注射了八种不同类型的携带mKO1基因的AAV载体。实验结果显示,AAV2.1-A载体在神经元内产生了更高水平的基因转导,无论是在转基因表达强度还是神经元数量方面。与其他载体相比,它展现出了更高的神经元特异性。

然后探究了拼接式AAV2.1-A和AAV2.1-B载体与原始AAV2和AAV1载体之间的基因转导特性以及神经元特异性。研究使用了不同类型的启动子评估了这些载体在神经元内的转基因表达水平和神经元特异性。结果显示,AAV2.1-A载体表现出最高效和最神经元特异性的基因转导,其神经元特异性甚至超过了AAV2载体,而AAV2.1-B载体在胶质感染性方面接近AAV1载体。然而,考虑到载体的胶质感染性,一些情况下转基因表达的信号可能不仅来自神经元,还来自胶质细胞。

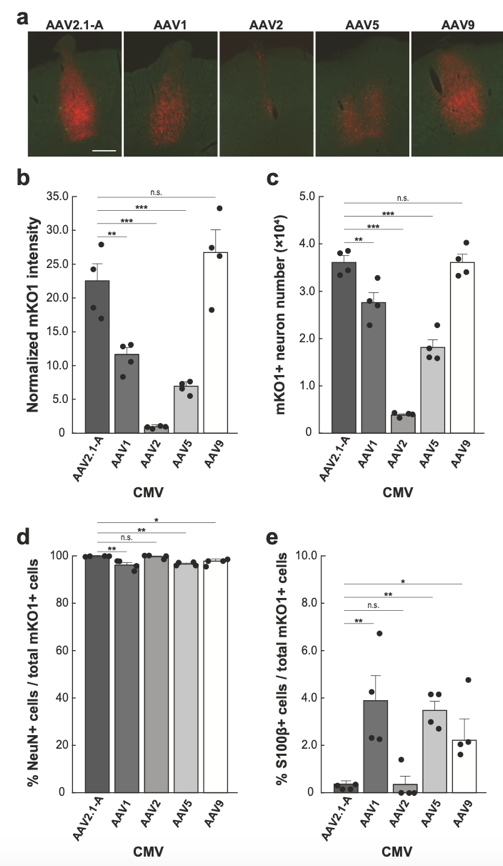
进一步比较了AAV2.1-A载体与AAV5和AAV9载体的基因转导特性。在实验中,我们注射了不同组合包膜的AAV-CMV-mKO1载体(AAV2.1-A、AAV1、AAV5和AAV9)以及具有相同病毒颗粒的AAV-Syn-mKO1载体到猴子的前额中央皮层。结果显示,AAV2.1-A载体在基因转导能力方面与AAV9载体相当,并在一些方面超越了AAV5载体。这些发现表明AAV2.1-A载体在大脑研究中具有潜在的优势。
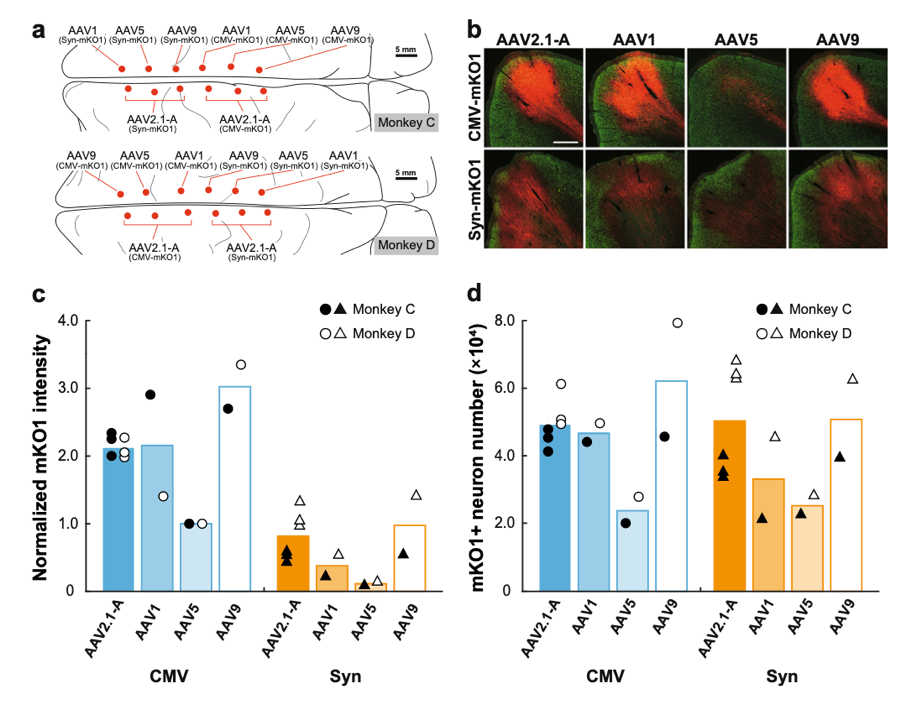
随后,分析了AAV5和AAV9载体与AAV2.1-A和AAV1载体的神经元特异性。结果显示,AAV2.1-A载体表现出最高的神经元特异性,而AAV5和AAV9载体则在一定程度上存在胶质感染。使用Syn启动子的载体几乎实现了完美的神经元特异性基因转导。

为了验证AAV2.1-A载体在啮齿动物大脑中的优越性是否适用于大脑,将其与AAV1、AAV2、AAV5和AAV9载体在大鼠大脑皮层中的基因转导特性进行了比较。结果显示,AAV2.1-A和AAV9载体在基因转导水平上表现出相似的高效率,且与AAV1、AAV2和AAV5载体相比,AAV2.1-A载体以及AAV2载体表现出更高的神经元特异性。
3. AAV2.1-A载体在化学遗传学操控方面的应用
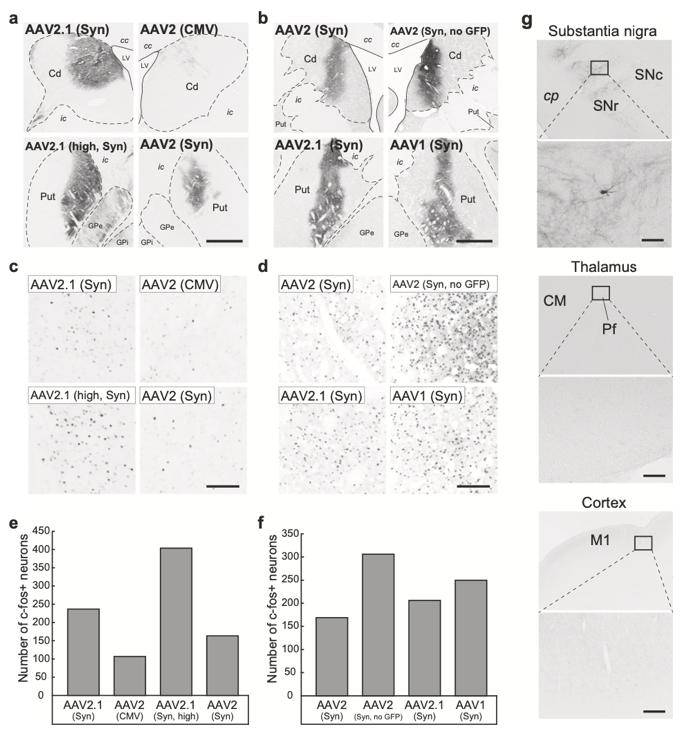
其次,研究者使用AAV2.1-A-Syn载体在大脑中进行化学遗传学调控实验。通过将修饰的人类M3毒蕈碱受体(hM3Dq)基因载入该载体,并在两只猕猴的纹状体注射,探索了受体结合、配体响应和转基因表达持续性等特性。与原始AAV2和AAV1载体进行比较,制备了不同的载体并应用不同的启动子,评估其在兴奋性DREADDs系统中的效能。
在第一只猴子中,将AAV2.1-A载体与AAV2载体进行比较,研究了其在DREADDs系统中的应用。注射了高度神经元特异性的载体,包括AAV2.1-A-Syn载体和其他类型的AAV载体,以评估DREADDs受体结合能力、配体响应和转基因表达持续性。结果显示,AAV2.1-A载体在[11C]DCZ结合(hM3Dq表达)和[18F]FDG摄取方面均表现出优越性,持续时间长达六个月以上。
在第二只猴子中,将四种类型的载体注射到纹状体,通过[11C]DCZ-PET和[18F]FDG-PET扫描,比较了AAV2.1-A载体与传统AAV2和AAV1载体的效果。结果显示,在不同时间点上,这些载体均展现出类似的高水平的[11C]DCZ结合和[18F]FDG摄取,持续时间达一年以上。
这些实验结果表明,AAV2.1-A载体在神经元活动的化学遗传学调控中具有优越性,为进一步的脑科学研究提供了有力工具。
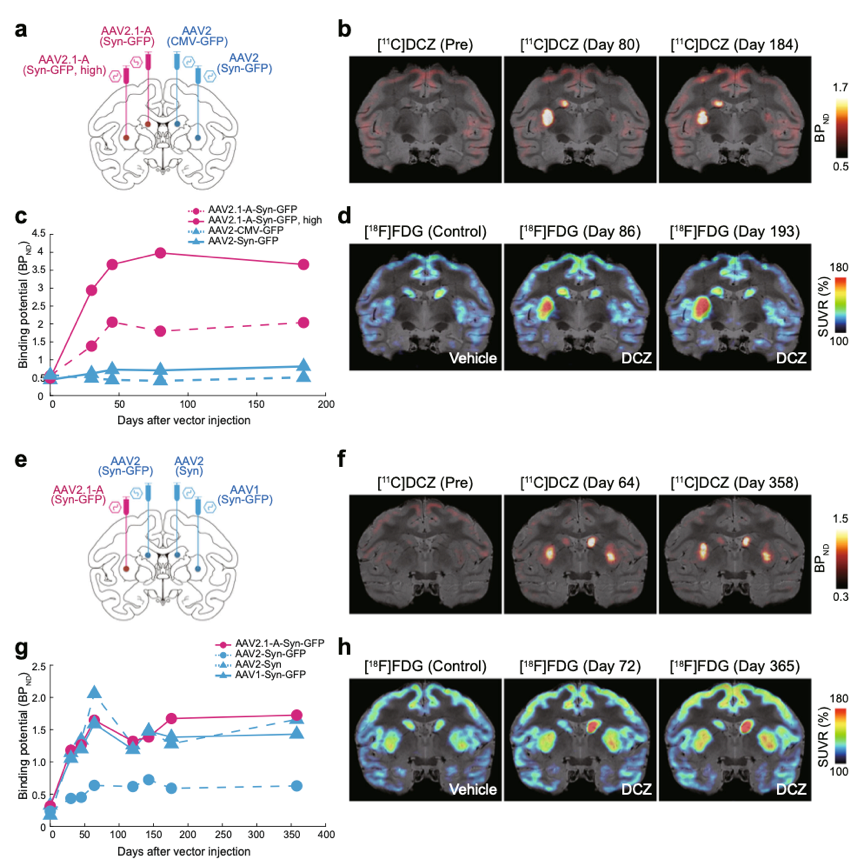
通过PET成像和免疫组织化学分析,证实了AAV2.1-A载体在纹状体中的神经元特异性表达。[11C]DCZ-PET成像显示hM3Dq表达与GFP阳性区域相符。DCZ处理后,AAV2.1-A载体在纹状体注射点表达c-fos的神经元数量显著增加。该载体偏向于从细胞体和树突摄取,同时在投射神经元和抑制神经元中表达转基因。
4. AAV2.1-A载体在体内钙成像中的应用
研究者使用融合载体进行光学成像研究,发现在猴子大脑皮层中可以稳定地监测神经元活动。这种载体产生高度选择性的转基因表达,对于神经元和胶质细胞具有高度特异性。同时,它在神经元中产生持久且稳定的荧光信号,可以长期监测活动。这为研究灵长类大脑的功能提供了有力工具。

研究 总结
这篇文章探讨了一种新型的病毒载体,用于在灵长类动物的大脑中实现基因转导和神经元活动监测。研究通过比较不同载体的特性,发现这种称为AAV2.1-A的载体在猴子和老鼠大脑中具有高度的神经元特异性和稳定的转基因表达能力。这种载体不仅对神经元产生持久的荧光信号,还可以在激活神经元活动时产生稳定的信号。因此,这项研究为深入理解灵长类大脑功能提供了有力的工具和方法。
