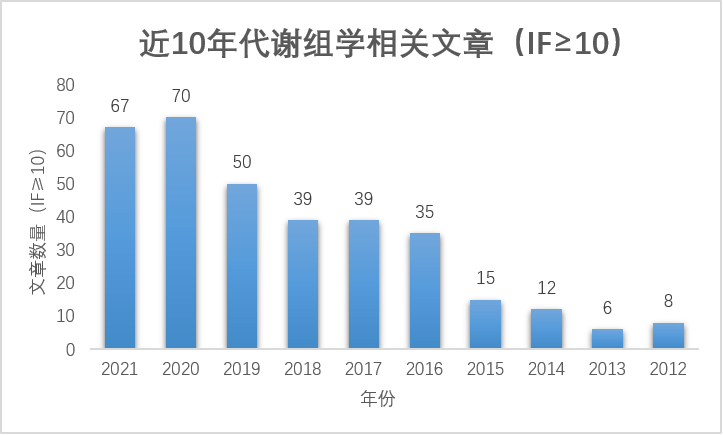
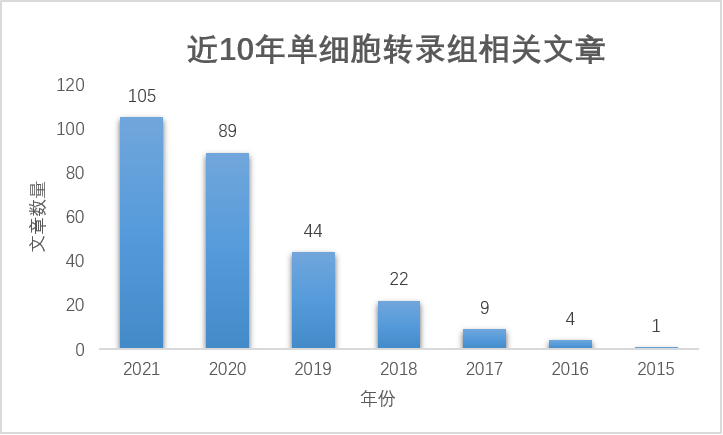
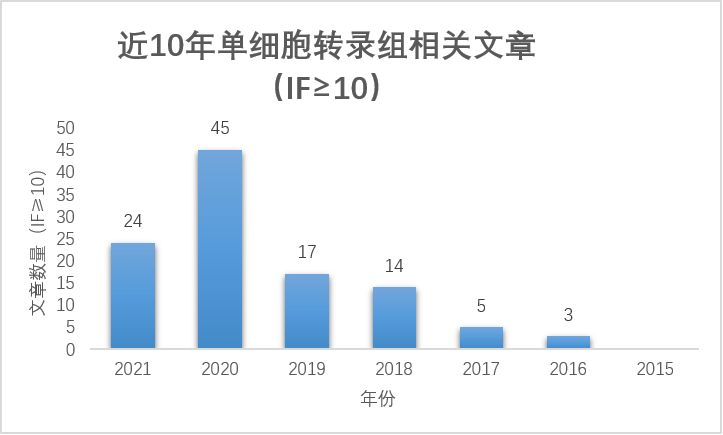
根据《中国心血管健康与疾病报告2020》,中国心血管病防治工作面临着严重挑战。据估计,全国心血管疾病患者高达3.30 亿,且患病率及死亡率仍处于上升阶段,并呈现年轻化。2018年,心血管病死亡率仍居首位,高于肿瘤及其他疾病。鉴于心血管疾病的极大危害性,开展相关心血管疾病防治的研究,对降低心血管病发病率、提高患者生活质量有着重要意义。今天,中科新生命为大家精心盘点了心血管领域组学研究进展及2021年高分精选文章简读,希望能为大家提供一些科研思路,也祝愿各位老师在2022年再创高峰。 据不完全统计,迄今为止,心血管领域涉及蛋白质组学文章,共发表6106篇,其中IF≥10的文章共671篇;2021年发表880篇,IF≥10的文章108篇,并且整体呈现出逐年递增的趋势,具体如下: 据不完全统计,迄今为止,心血管领域涉及代谢组学文章,共发表2900篇,其中IF≥10的文章共323篇;2021年发表583篇,IF≥10的文章67篇,并且整体呈现出逐年递增的趋势,具体如下: 3 单细胞转录组 据不完全统计,迄今为止,心血管领域涉及单细胞转录组文章,共发表263篇,其中IF≥10的文章共104篇;2021年发表105篇,IF≥10的文章24篇,值得关注的是,单细胞转录组的研究热度近两年持续升高(2015年之前未统计到相关文章),具体如下: 精选文献简读 1 文献名称:Fat-Secreted Ceramides Regulate Vascular Redox State and Influence Outcomes in Patients With Cardiovascular Disease 发表期刊:J Am Coll Cardiol(IF=24.094) 组学技术:代谢组学 实验材料:CABG手术肥胖和非肥胖患者的胸腔脂肪(ThAT)和皮下脂肪(ScAT) 技术路线: · 1 代谢组学:SPL代谢是肥胖中ThAT分泌组中显著失调的代谢途径; · 2 ThAT和ScAT之间神经酰胺分泌和产生水平的差异(靶向代谢-SPL相关代谢物); · 3 细胞实验:原代脂肪细胞通过细胞外囊泡产生和释放 SPL; · 4 高水平的 ThAT 衍生的 SPL 与人体血管中,O2.−产量增加和内皮功能受损有关; · 5 血浆 Cer16:0 水平升高与人类动脉氧化应激、内皮功能障碍和全身炎症增加有关; · 6 Cer16:0 对内皮氧化还原状态的直接影响; · 7 血浆 Cer16:0 水平预测心脏死亡率。 小结: 本研究作者招募了48位患有动脉粥样硬化的肥胖患者,采集其胸部脂肪组织(ThAT)和皮下脂肪组织,利用代谢组学分析两处脂肪组织的代谢差异。并将组学结果与之前633例行CABG手术患者的血管氧化还原信号进行关联分析。结果显示,ThAT与皮下AT中鞘脂分泌存在显著差异,其中C16:0-神经酰胺及其衍生物是在脂肪细胞来源的外泌体重具有显著差异。此外,作者进一步证实高血浆C16:0-神经酰胺及其糖基化衍生物与心源性死亡风险增加独立相关。总而言之,该研究首次在人类中证明,脂肪组织来源的神经酰胺是肥胖个体血管氧化还原状态的可调节的调节剂,直接影响晚期动脉粥样硬化患者的心源性死亡率。 2 文献名称:Myeloid-Derived Growth Factor Protects Against Pressure Overload-Induced Heart Failure by Preserving Sarco/Endoplasmic Reticulum Ca2+-ATPase Expression in Cardiomyocytes 发表期刊:Circulation(IF=29.69) 组学技术:单细胞测序,蛋白组学和磷酸化蛋白组学 实验材料:小鼠心肌、炎症细胞、血浆和人血浆 技术路线: · 1 构建MYDGF基因编辑细胞和小鼠模型代; · 2 MYDGF表达与功能分析; · 3 蛋白组学和磷酸化蛋白组学分析MYDGF的信号靶点; · 4 分子实验揭示MYDGF保护心力衰竭的作用机制。 小结: 本研究构建了MYDGF基因编辑细胞和小鼠模型,发现MYDGF具有保护压力超负荷诱导的心力衰竭的功能,通过蛋白组学和磷酸化蛋白组学技术检测MYDGF调控的下游的蛋白表达情况和磷酸化修饰位点变化情况,确定PIM1激酶为心肌细胞MYDGF的信号靶点,最后又通过基因功能研究阐述MYDGF在心力衰竭发病机制中的调控机理,为心力衰竭的预防治疗提供了新的思路。 3 文献名称:Pharmacological inhibition of arachidonate 12-lipoxygenase ameliorates myocardial ischemia-reperfusion injury in multiple species(客户文献) 发表期刊: Cell Metab (IF=27.287) 组学技术:代谢组学 实验材料:19名心肌梗死的临床患者的冠状动脉介入手术(PPCI)前后的血浆样本 技术路线: · 1 代谢组学分析发现12-HETE是MIR损伤发生中的关键代谢物; · 2 12-HETE合成酶ALOX12与MIR损伤调控有关; · 3 ALOX12小分子抑制剂ML355可以改善MIR造成的心肌损伤; · 4 ALOX12可加强泛素化酶NEDD4作用导致TAK1降解; · 5 ML355干扰ALOX12-NEDD4-TAK1复合物形成。 小结: 本研究通过非靶代谢组学对心肌梗死患者冠状动脉介入(PCI)术前术后血浆样本代谢表型变化进行检测,发现12-HETE是缺血再灌注损伤的重要标志物。明确12-HETE对应合成酶ALOX12是心脏缺血再灌注损伤的重要调控靶点及其调控机制。并在小鼠及高等动物模型中一致证明ALOX12的小分子抑制剂可以有效改善缺血再灌注损伤,研究为后续临床转化提供了可能。 解读详情: 4 文献名称:Systems Approach to Discovery of Therapeutic Targets for Vein Graft Disease 发表期刊: Circulation(IF=29.69) 组学技术:单细胞测序、Label free蛋白组学、代谢组学 实验材料: · 单细胞转录组学测序:体外刺激的人原代巨噬细胞 · 蛋白组学:不同背景/喂养方式、不同模型时间点小鼠静脉移植静脉和对照下腔静脉组织 · Metabolon代谢组学:体外刺激的人原代巨噬细胞(含分离线粒体) 技术路线: · 1 小鼠静脉移植模型构建与表型观察; · 2 小鼠模型移植静脉组织的Label free蛋白组学检测; · 3 蛋白结果网络分析筛选潜在靶点——PPARα; · 4 巨噬细胞PPARα SiRNA沉默——加速静脉移植病变发展,巨噬细胞PPARα激活可减轻静脉移植的病变负担和炎症水平; · 5 疾病网络临近分析:关联静脉移植蛋白质组学网络与人类AVF疾病网络; · 6 PPARα激活可减少小鼠实验性AVF病变大小并增加其通畅性(体内); · 7 PPARα激活减轻小鼠巨噬细胞促炎性激活(体外); · 8 单细胞转录组学揭示促炎性巨噬细胞独特的炎症细胞群; · 9 代谢组学分析证实PPARα激活可以影响巨噬细胞代谢重编程、线粒体功能和氧化损伤。 小结: 本研究作者系统剖析静脉移植病变发展(静脉动脉化导致的主要临床问题),并建立一个分析平台(涉及蛋白质组学和网络分析)。接着,作者从核心网络中选择一个众所周知的PPARα途径,利用体内外模型、结合激活和沉默实验,证实PPARα确实通过影响巨噬细胞功能在静脉移植疾病中发挥抗粥样硬化、抗炎作用。此外,作者还发现PPARα激活还减轻了另一种静脉适应性不良障碍AVF的疾病发展。综上,本研究通过整合单细胞测序、蛋白组学和代谢组学平台,结合多种体内外动物模型,增加了我们对于静脉移植疾病的了解,证实作者开发平台的可信度,并未PPARα靶向治疗这一重大健康负担提供分子基础。 5 文献名称:BET Inhibition Blocks Inflammation-Induced Cardiac Dysfunction and SARS-CoV-2 Infection 发表期刊:Cell(IF=38.637) 组学技术:单核RNA测序、磷酸化蛋白组学 实验材料:多细胞人类多能干细胞 (hPSC) 衍生的心脏类器官 (hCOs) 小结: 本研究作者基于人类多能干细胞(hPSC)衍生出的心脏类器官模型,结合磷酸化蛋白组学和单核RNA测序技术,发现SARS-CoV-2感染诱导的心脏舒张功能障碍的炎性“细胞因子风暴”,是由于干扰素γ、IL-1β和聚(I:C)的联合作用。此外,作者通过功能学实验证实BET抑制剂通过降低病毒应答中的基因转录、降低COVID-19受体(ACE2)表达,帮助恢复心脏类器官的舒张功能。最终证实,包括Apabetalone在内的BET抑制剂有望成为预防新冠诱导的心脏损害的候选药物。 6 文献名称:A proteomic atlas of the neointima identifies novel druggable targets for preventive therapy 发表期刊: European Heart Journal(IF=29.983) 组学技术:蛋白质组学 实验材料:小鼠股动脉样本(金属丝损伤/对照) 技术路线: · 1 金属丝损伤不同时间点的蛋白组学检测; · 2 组学分析:揭示血管损伤对小鼠核心基质体及其相关蛋白影响; · 3 组学分析:新生内膜形成过程中迁移因子的调控; · 4 体内实验:证实Trpc6对小鼠新生内膜形成的影响; · 5 体外实验:证实Trpc6可作为调节人血管平滑肌增殖迁移的潜在靶点。 小结: 本研究作者构建了金属丝诱导的小鼠股动脉损伤模型(不同时间点),利用蛋白组学解析小鼠股动脉新生血管内膜形成过程中的蛋白表达变化。结果显示,在血管损伤后不同时间点,主要是细胞外基质的重构以及细胞迁移因子的改变,并从中筛选出一个驱动新生内膜形成的蛋白(TRPC6)。接着,作者在KO小鼠和细胞实验中证实其对于新生内膜形成和平滑肌细胞迁移或增殖的重要作用。此外,作者利用大队列基因组学分析发现,携带TRPC6变异的纯合子患者冠脉支架术后再狭窄风险增加。值得注意的是,TRPC6抑制剂或许可作为涂层,应用在支架表面,从而减轻支架内再狭窄。 7 文献名称:Extracellular Matrix in Heart Failure: Role of ADAMTS5 in Proteoglycan Remodeling 发表期刊: Circulation(IF = 29.69) 组学技术:蛋白质组学,单细胞测序 实验材料:心力衰竭患者和未衰竭对照心脏的左心室组织 技术路线: · 1 蛋白组学1:揭示缺血性HF患者瘢痕心肌的ECM组成; · 2 动物实验1:ADAMTS5介导Versican裂解; · 3 动物实验2:Adamts5 ΔCat小鼠的心脏功能; · 4 单细胞测序:Versican和ADAMTS在人类心脏中表达; · 5 蛋白组学2:药物对缺血性HF中ECM成分的影响; · 6 体外实验:去甲肾上腺素在CF中诱导Versican表达。 小结: 本研究作者使用蛋白质组学分析了来自80名心衰患者和6名未心衰患者(对照)心脏的左心室组织,这是迄今为止对人类心衰进行的最大的蛋白组学分析。作者通过证明多聚糖和其他蛋白聚糖也在缺血性 HF 患者的瘢痕心肌中积聚,证实了之前在 I/R 损伤猪模型中的发现。接着,作者证实 ADAMTS 蛋白酶在心脏重塑过程中裂解多功能蛋白聚糖。此外,作者证明了 Adamts5ΔCat小鼠中多功能蛋白聚糖的积累与心脏功能受损和参与细胞间通讯的蛋白质减少有关。最后,作者探讨了药物对 ECM 重塑的影响,并揭示了 β-受体阻滞剂减弱了缺血性 HF 中的多聚糖积累。 8 文献名称:Untargeted metabolomics identifies succinate as a biomarker and therapeutic target in aortic aneurysm and dissection 发表期刊:European Heart Journal(IF=29.983) 组学技术:非靶向代谢组学、靶向代谢组学 实验材料:AAD患者血浆 技术路线: · 1 非靶向+靶向代谢组学:AAD患者血浆中琥珀酸含量增加; · 2 生信分析:琥珀酸作为新型AAD标志物; · 3 动物实验1:补充琥珀酸加重AAD进展; · 4 动物实验2:干预OGDH抑制巨噬细胞炎症反应; · 5 动物实验3:敲低CREB降低巨噬细胞炎症反应; · 6 动物实验4:特异性敲低P38a减轻AAD进展。 小结: 本研究作者通过非靶向代谢组学和靶向代谢组学,分别在两个AAD队列及健康对照人群中证明AAD患者血浆中琥珀酸水平显著升高;并结合临床资料分析,证明琥珀酸可作为诊断AAD的新型标志物。接着,作者在AAD动物模型中外源性补充琥珀酸(饮水中添加),证实琥珀酸可加重不同造模方式小鼠的AAD程度。此外,作者针对调控琥珀酸生成的关键酶——α-酮戊二酸脱氢酶(OGDH),发现敲低或者抑制OGDH可降低琥珀酸水平并抑制巨噬细胞炎症反应。作者还结合CHIP技术筛选调节OGDH的转录因子CREB,发现敲低CREB可通过减少OGDH表达降低巨噬细胞炎症因子分泌。最后,作者发现p38a调控CREB磷酸化从而增加OGDH表达以及琥珀酸累积,并通过髓系特异性敲除p38a证实上述发现。 2021年已成为过去,祝愿广大科研工作者2022年再迎科研硕果,共创学术佳绩! 此外,各热门领域2021年终盘点正在进行,持续关注,更多精彩盘点,敬请期待!
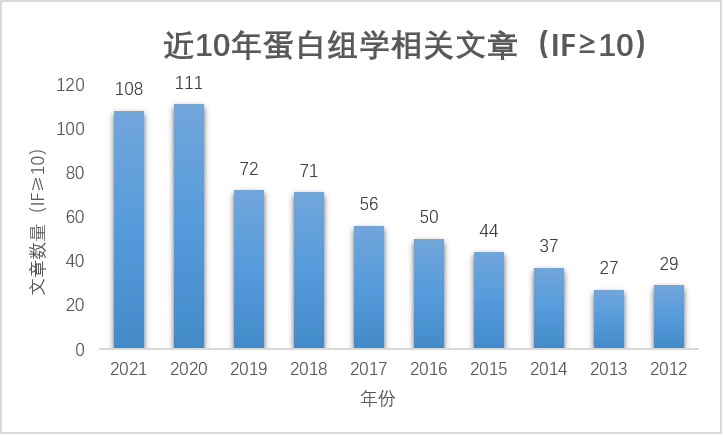
1 蛋白质组学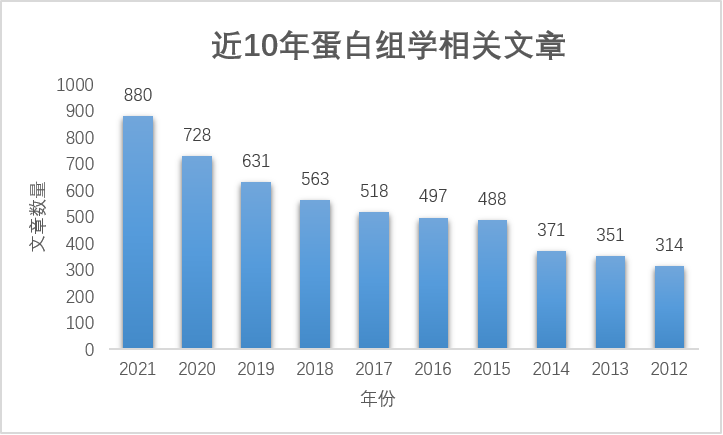
2 代谢组学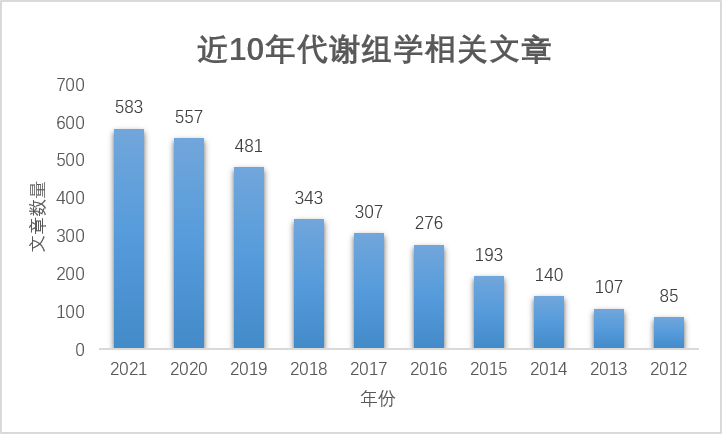
年终盘点 | 一文回顾2021年心血管领域组学研究进展
作者:上海中科新生命生物科技有限公司 2022-01-05T11:39 (访问量:2939)
上海中科新生命生物科技有限公司 商家主页
地 址: 上海市园美路58号1号楼15-18楼
联系人: 徐
电 话: 021-54665263
传 真:
Email:marketing@aptbiotech.com
相关咨询
会议邀请 | 第8届全国植物蛋白质研究大会暨首届贵阳生命科学新高地科学家论坛 (2023-07-07T14:37 浏览数:13906)
项目文章Cell(IF 64.5)| 中国科技大学探索食物过敏谜团 (2023-07-07T14:22 浏览数:14093)
Gastroenterology(IF 29.4)| 基于机器学习算法开发的外泌体miRNA生物标志物用于胰腺导管腺癌早期诊断 (2023-07-05T15:54 浏览数:11701)
Cancer Letters(IF 9.7)|天津市环湖医院利用Labelfree揭示超声-替莫唑胺联合诱导胶质瘤细胞的凋亡机制 (2023-06-30T09:37 浏览数:12754)
Excel表免费下载 | 速来围观!2023年影响因子发布 (2023-06-29T09:35 浏览数:11456)
外泌体多组学创新解决方案,精准、前沿的疾病诊断生物标志物 (2023-06-28T10:20 浏览数:15697)
Immunity (IF=43.474)丨单细胞+空间联合揭示肉芽肿形成的异常淋巴发育进程 (2023-06-26T17:28 浏览数:11849)
专家齐聚 亮点回顾 | 2023年海口·中医药创新多组学研究论坛圆满落幕 (2023-06-25T10:10 浏览数:16439)
项目文章Plant J(IF 7)| 杭州师范大学王慧中团队通过空间代谢+单细胞测序等揭示红豆杉幼茎细胞特异的紫杉烷合成调控模式 (2023-06-25T09:42 浏览数:13984)
项目文章Gut Microbes(IF 9.434)| 肠道微生物竟是导致胆囊切除术后患者腹泻的元凶? (2023-06-14T16:35 浏览数:11392)
