炎性乳腺癌(IBC)是一种高度侵袭性的恶性肿瘤,具有独特的临床和组织病理学特征,但其分子基础尚未剖析清楚。
美国科学家评估了一个IBC细胞系A3250,它在小鼠异种移植瘤模型中再现了关键的IBC特征。研究者使用转录组RNA测序和Olink Target 96炎症panel明确了A3250细胞表达高水平的CCL2趋化因子,且是驱动巨噬细胞扩张的关键因子,并间接促进了肿瘤的生长。总体,基于A3250的IBC模型将为探索IBC独特生物学提供新的见解。研究成果以“High endogenous CCL2 expression promotes the aggressive phenotype of human inflammatory breast cancer”为题,发表在Nature Communication(中科院JCR一区,IF:14.919 )上。
研究结果
1. 通过原发肿瘤分离建立了一种炎症性乳腺癌A3250,具有侵袭转移特性
A3250乳腺癌细胞系是从一个三阴性炎性乳腺癌(IBC)患者的原发肿瘤中分离并构建的细胞系。STR分析证实该系是独特的,任何现有STR谱的相似性低于55%。A3250细胞表现出比通常研究的三阴性乳腺癌(TNBC)系MDA-MB-231细胞更高的集落形成能力。A3250缺乏雌激素或孕激素受体(ER或PR),HER2(人类表皮生长因子受体-2,ERBB2)mRNA水平与其他TNBC细胞系相当。与MCF7或BT474肿瘤相比,A3250原位肿瘤也缺乏ER、PR或HER2蛋白。这些数据证实A3250是TNBC细胞系。A3250人异种移植瘤模型显示了人IBC关键的临床和组织病理学特征,也保留了人类IBC的关键特征:A3250原位肿瘤会自发地转移到多个器官,如在6周内转移到前哨淋巴结(腹股沟)或更远的淋巴结(腋窝和肱)。A3250肿瘤也显示出向肺和肝转移的高发生率(89%)。研究表明,A3250来源的肿瘤再现了人类IBC的侵袭性转移表型。
2. 转录组学分析揭示了A3250细胞中与炎症相关的多种通路的激活
为了深入了解侵袭性IBC表型的潜在驱动因素,研究者对A3250细胞进行了转录组学分析。将A3250的基因表达谱与6个人TNBC细胞系(2个IBC和4个非IBC)进行了比较。分层聚类显示,A3250细胞与SUM149 IBC细胞最接近。
IPA分析显示,与MDA-MB-231细胞相比,A3250在与炎症相关的通路中表现出显著的富集,A3250有10个典型通路被激活,其中8个与炎症相关。与IBC3相比,A3250显示了与纤维化、EMT和细胞骨架等相关的通路的激活。与MDA-MB-231和IBC3相比,A3250中PI3/AKT信号通路和肿瘤微环境被激活,信号素信号通路失活。与SUM149相比,A3250仅显示5条通路富集,其中与脂质代谢和炎症相关的LXR/RXR典型通路上调最为显著。
基因集富集分析(GSEA)分析显示,A3250与MDAMB-231相比有34个基因集显著富集,与IBC3相比有31个基因集显著富集,与SUM149相比有22个基因集显著富集。在与炎症相关的通路中,与MBA-MB-231、IBC3和SUM149相比,通过NF-κB的标志性“TNFA信号”在A3250中显著富集。A3250相比MDA-MB-231和IBC3也存在JL6 JAK STAT3信号的富集。总体,IPA和GSEA分析表明A3250中多种炎症通路的激活。

3. A3250 IBC肿瘤引起明显的局部和全身炎症
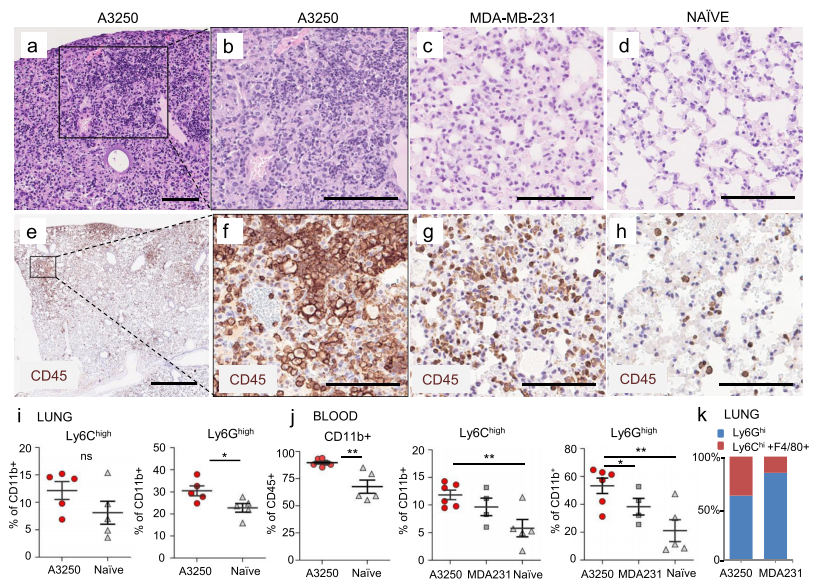
病理学家对IBC中炎症浸润的程度和意义有不同的看法,人们普遍认为炎症是癌细胞堵塞真皮淋巴管的结果。因此,研究者试图与淋巴管浸润(LVI)相比,描述A3250肿瘤中炎症细胞积累的动力学。免疫染色显示炎症细胞在肿瘤侵袭皮肤淋巴管之前就已经积累了。丰富的炎症细胞富集可能是由于肿瘤来源的细胞因子的积极招募,而不是由于肿瘤栓塞阻塞淋巴管引起的。免疫染色进一步显示,在整个存活的A3250肿瘤和邻近的真皮中,F4/80+巨噬细胞的密度非常高。注射后4周检查了携带A3250肿瘤的小鼠的肺,H&E染色显示肺结构异常,其特征是密集的炎症浸润和肺泡结构缺失。流式细胞结果显示,与无肿瘤小鼠肺相比,Ly6Chi髓系细胞有增加趋势、血液中总CD11b+细胞、Ly6Chi炎症单核细胞和Ly6Ghi中性粒细胞的比例显著增加。
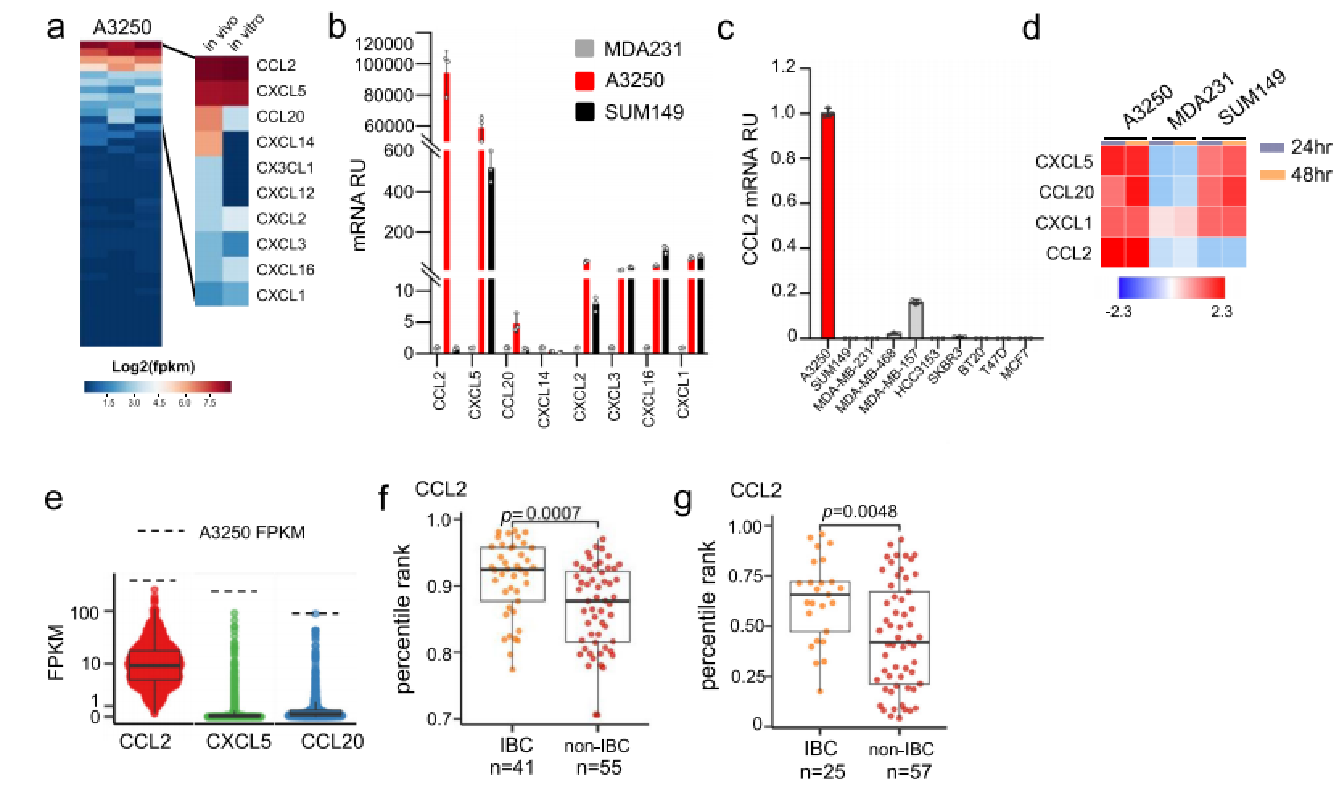
4. CCL2在A3250细胞和人IBC中高表达
为了确定可能介导A3250肿瘤髓细胞招募的原因,研究者分析了A3250肿瘤和细胞mRNA-Seq结果中趋化因子的表达。A3250肿瘤的结果分析显示,44个趋化因子中10个有表达,其中只有3个(CCL2、CXCL5和CCL20)在肿瘤(体内)和细胞(体外)均高表达,而CCL2的表达量最高。随后,研究者利用Olink Target 96炎症panel检测了A3250细胞上清中的趋化因子,其中CCL2、CXCL5和CCL20蛋白水平较高。研究者分析了包含41个人类IBC和55个非IBC的Van Laere芯片数据,以及包含25个IBC和57个非IBC 的Iwamoto数据。在两个数据集中,IBC的CCL2中位数表达水平均显著高于非IBC。综上所述,这些数据表明,人类IBC,如A3250,通常表现出较高的CCL2表达水平。
5. 趋化因子受体CCR2在A3250 IBC肿瘤模型的髓系细胞高表达
趋化因子CCL2通过CCR2发挥作用,CCR2是主要的趋化因子受体,介导单核细胞和巨噬细胞招募到炎症部位。研究者检测了CCR2在A3250肿瘤、肺和血液的白细胞中的表达情况。结果表明,血液中存在高水平的CCR2+炎症单核细胞和高CCR2表达的髓系细胞与A3250肿瘤和肺转移相关。虽然CCL2在A3250细胞中高表达,但其他激活CCR2的人类趋化因子(CCL7、CCL8、CCL13和CCL16)均未表达。这些发现表明,在A3250肿瘤模型中,CCL2作为关键的CCR2激动剂,并强烈提示CCL2在单核细胞和巨噬细胞招募到A3250原发和转移位点中发挥重要作用。

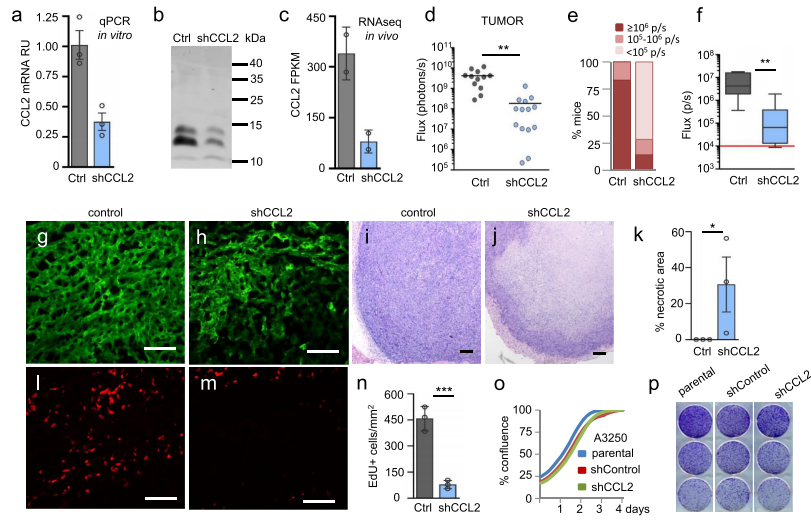
6. CCL2敲低显著降低了A3250肿瘤的生长、肺转移和炎症表型
为了研究CCL2在A3250肿瘤恶性表型中的功能,研究者对CCL2进行了shRNA敲低(KD)。CCL2敲低可显著抑制肿瘤生长,同时IBC特征的皮肤炎症也显著减少。此外,CCL2敲低降低了肺转移的发生率和总体转移负担。大多数CCL2敲低肿瘤小鼠肺内无大转移,主要表现为弥散性肿瘤细胞,而对照组A3250肿瘤小鼠主要表现为大转移。
CCL2敲低肿瘤免疫细胞的免疫染色显示,肿瘤区域的CD45+细胞显著减少,其中大部分是F4/80+巨噬细胞。肿瘤中CCL2的下调可减少巨噬细胞浸润和全身炎症。
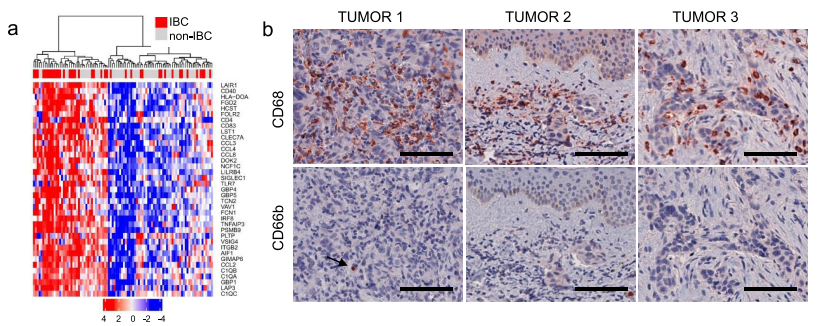
7、 人IBC存在巨噬细胞的富集
最近的一项研究发现了基于不同免疫浸润的不同人类TNBC(三阴性乳腺癌)亚型,从巨噬细胞富集到中性粒细胞富集。为了检验人类IBC是否富含巨噬细胞,研究者分析了41个人类IBC和55个非IBC的芯片数据。分层聚类显示了两类乳腺癌,分别为富集或不富集TAM(肿瘤相关巨噬细胞)基因。富集TAM基因的IBC样本明显多于未富集TAM基因的IBC样本。免疫染色检测巨噬细胞(CD68+)和中性粒细胞(CD66b+)显示,高密度巨噬细胞出现在间质和/或肿瘤细胞簇内。该结果与基因表达分析表明人IBC存在巨噬细胞富集,也与研究者对A3250肿瘤的研究结果一致,进一步强调了A3250肿瘤模型与人IBC的相关性。
研究总结
本研究围绕一个来源于三阴性炎性乳腺癌(IBC)的细胞系A3250进行了研究。A3250细胞及移植瘤模型显示了人IBC关键的临床和组织病理学特征。对A3250细胞和肿瘤的转录组RNA测序发现了显著的炎性特征,结合Olink Target 96炎症panel找到了一个在A3250细胞和肿瘤中高表达的趋化因子CCL2,该趋化因子在IBC的原发和转移位点发挥关键作用。敲低CCL2可有效改善移植瘤小鼠的疾病特征。此外,研究者发现,在巨噬细胞是临床IBC中的一个主导亚群,这意味着耗尽或靶向巨噬细胞的免疫治疗策略可能是很有前途的IBC治疗方法。总体,本研究的结果表明,基于A3250细胞的IBC肿瘤模型将帮助人类进一步了解IBC生物学,并有助于促进IBC靶向治疗方法的开发。
吉凯基因凭借多年在靶标筛选及验证服务领域的技术积累,建立的标准化 、工程化 、系统化的GRP平台,为中国研究型医生提供科研服务,加快科研成果转化。其中,多组学平台包含蛋白质组学平台和高通量测序平台:
·蛋白质组学平台拥有多台timsTOF Pro、Exploris 480高精度质谱仪,专业的Spectronaut Plusar、Mascot等分析软件,提供专业的4D、DIA、TMT、PRM、磷酸化修饰组、olink蛋白质组等检测服务,强大的机器学习算法、IPA分析、蛋白基因组分析服务,系统的生物标志物、分子分型、药物靶点、基因功能研究等解决方案,真正让广大研究型医生的科研工作更省心、更省力、更高效;
·高通量测序平台分为常规测序服务和单细胞测序服务:单细胞测序拥有10x和BD两个平台,提供单细胞RNA-seq、单细胞核测序、单细胞混样RNA-seq、单细胞TCR/BCR、单细胞(RNA+ATAC)、空间转录组测序等服务;常规测序服务提供meRIP-seq(m6A/m1A/m7G/m5C 等RNA甲基化修饰测序)、acRIP-seq(ac4C RNA乙酰化修饰测序)、ATAC-seq、Ribo-seq(翻译组测序) 、mRNA/miRNA/LncRNA/circRNA-seq、全转录组测序(两文库/三文库)、外泌体miRNA/LncRNA-seq、WGS/WES、WGBS、RRBS、BSAS等服务。
