肿瘤坏死因子(TNF)通路是一个高度依赖蛋白质磷酸化调控的重要的促炎信号通路。临床上,靶向TNF在治疗炎症方面非常成功,但抗炎疗法可能会引起严重的副作用。由于TNF相关磷酸化调控网络未得以全面剖析,因此亟需更系统的方法深入了解其中激酶、磷酸酶、底物关系及其信号转导动力学变化,为药物干预提供靶点,帮助更精确地控制疾病。 今年10月,蛋白组学领军大牛Matthias Mann教授团队在Nature Communications上发表了题为 “Phosphoproteome profiling uncovers a key role for CDKs in TNF signaling”的论文,利用高深度的DIA磷酸化蛋白质组学深入解析了TNF下游的信号转导变化,从功能上探讨了TNF及其诱导的细胞死亡中蛋白磷酸化变化,并揭示了CDK激酶在其中的关键调控作用,为抗炎治疗等提供潜在药物干预靶点。 技术路线 步骤1:通过DIA磷酸化组学,比较TNF处理不同时间磷酸化水平的变化; 步骤2:抑制关键激酶并揭示激酶和底物的关系; 步骤3:分离细胞膜、细胞核和细胞质,通过组学研究TNF诱导的磷酸化引起的蛋白易位; 步骤4:研究TNF诱导的细胞死亡中蛋白和磷酸化水平的变化; 步骤5:抑制CDK激酶,通过蛋白组学研究CDK的作用。 研究结果 1. TNF诱导磷酸化水平随时间变化,可区分早期和晚期信号转导活动 为系统描绘TNF相关磷酸化变化网络,对TNF处理不同时间后U937细胞进行DIA磷酸化蛋白质组学分析,共鉴定到28,000条高可信度的磷酸化肽段。结果显示,磷酸化水平在处理3min后显著上调,15min达到峰值,大多数在60min后恢复到基线水平(图1d,e,f)。进一步分析表明,许多参与NF-κB、模式识别信号通路为瞬时变化修饰蛋白,少数转录相关蛋白为较为持久修饰蛋白,其磷酸化在TNF刺激后60分钟仍保持上调 (图1f)。综上,可根据蛋白磷酸化变化时序区分早期(5分钟)、中期(15分钟)、晚期(60分钟)信号活动。 图1 TNF调控下不同时间的磷酸化信号活动 2. TNF刺激下的激酶-底物关系分析 为进一步揭示激酶-底物关系,使用特定抑制剂去抑制关键激酶活性,并进行磷酸化组学分析。结果表明,对于通过激活NF-κB等上游通路的激酶而言,如TAK1,其活性抑制后几乎消除了TNF相关的磷酸化变化(图2c)。相反,抑制下游激酶如IKK1/2、p38、MEK1/2和JNK则不能完全消除TNF作用(图2c)。进一步在STRING网络中分析激酶与底物关系,发现在TNF刺激下磷酸化的蛋白质并未与其他磷酸化蛋白紧密相关 (图2d)。同时,有些蛋白不受TAK1抑制影响,但受到IKK1/2抑制的强烈影响(图2e),表明IKK1/2发挥了一些不依赖于TAK1活性的功能。总之,该分析全面揭示了TNF刺激下的激酶与底物关系。 图2 TNF刺激下的激酶-底物关系 3. TNF相关磷酸化引发蛋白质重新定位 TNF相关磷酸化变化依赖于激酶及其底物的重新定位。为了分析该现象,比较TNF处理后,细胞膜、细胞核和细胞质中的蛋白及磷酸化变化,从而评估蛋白质定位变化 (图3a)。结果显示,NF-κB通路、转录相关蛋白质等很多蛋白质发生定位变化(图3d,e, f)。富集分析显示,RIG-I通路、RNA加工体组装的蛋白质在膜上发生磷酸化变化,而模式识别受体信号通路和细胞迁移通路中的磷酸化在细胞质基质中发生变化(图3h),且其中多数能被TAK1抑制剂阻碍,暗示其受细胞质中TAK1 活性调控(图3g)。 图3 TNF诱导的磷酸化影响TAK1下游信号通路成员的定位变化 4. TNF诱导的细胞死亡触发强烈的RNA加工响应和CDK激活 为分析TNF诱导细胞死亡中关键调控的磷酸化蛋白,对TNF处理的U937细胞添加细胞凋亡和坏死抑制剂(SM、IDN-6556)诱导细胞死亡,并进行磷酸化组学分析 (图4b)。结果表明,RNA剪接和mRNA加工的蛋白磷酸化在凋亡过程中显著上调(图4c)。进一步分析及验证发现,该过程受到细胞周期蛋白依赖激酶CDKs的磷酸化变化调控,CDKs通过调节RNA聚合酶II活性来调节转录过程, 其中,CDK9 T354位点的磷酸化在TNF处理后上调9倍(图4c-i)。 图4 TNF诱导的细胞死亡导致强烈的RNA加工响应及CDK激活 5. TNF靶基因的转录依赖于CDK激酶活性 TNF能诱导广泛的靶基因转录表达,而上述分析中已发现CDKs通过调节RNA聚合酶II活性调控转录。为进一步解析CDKs活性变化是否影响TNF诱导的靶基因表达。采用不同CDKs抑制剂处理TNF刺激的U937细胞,并进行蛋白质组分析,发现CDK激酶活性抑制后几乎消除了TNF诱导的蛋白质表达变化(图5a-5b)。随后,又验证了相关靶基因CCL2 (MCP1)和CXCL10 (IP10)mRNA水平变化,发现同样下调(图5d),说明该过程确实发生在转录水平上。综上表明,CDKs激酶活性变化调控TNF靶基因的转录。 小结 中科优品推荐 磷酸化修饰是生物体内最普遍的一种修饰,研究方法众多,【中科新生命】可提供4D-labelfree、TMT、DIA多种技术方法的磷酸化组学检测。其中DIA磷酸化可实现超高深度的检测,覆盖度及准确性都有显著提升。欢迎感兴趣的老师前来咨询。

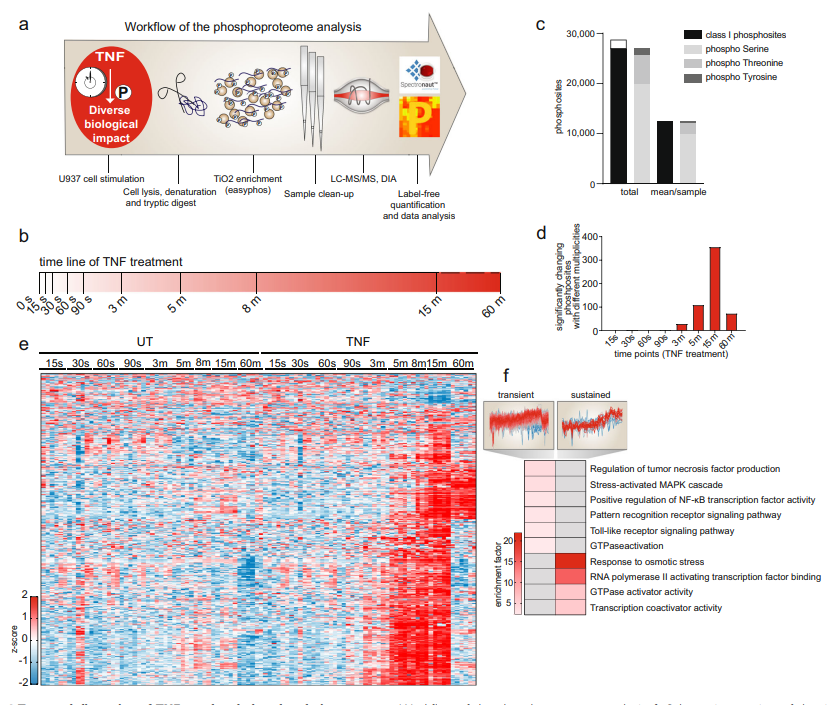
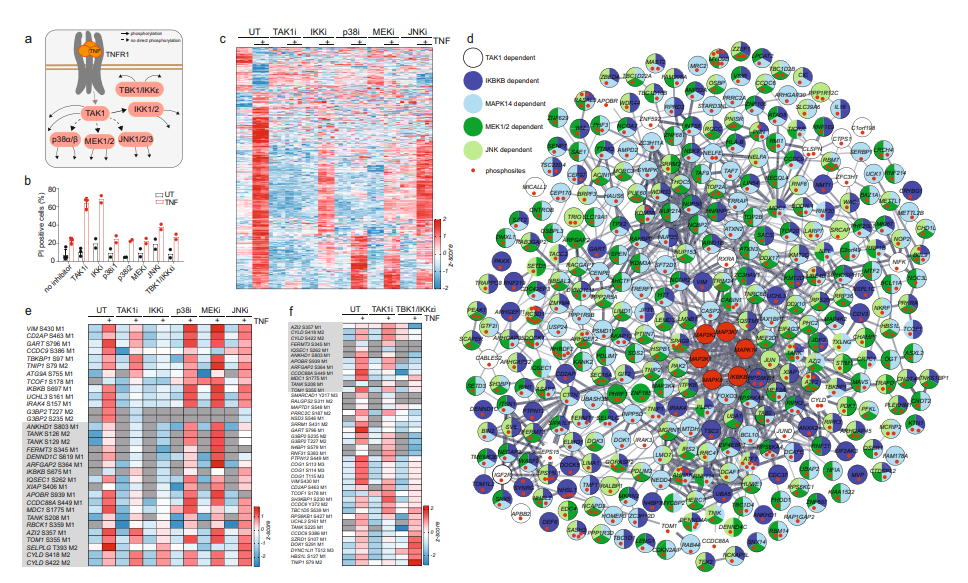
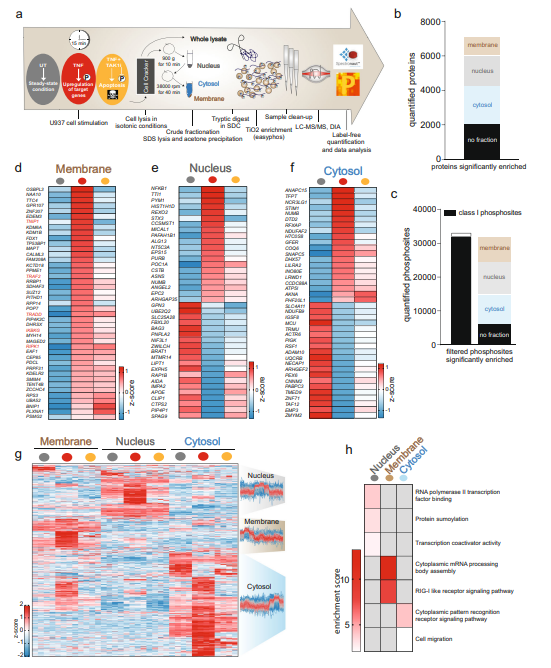
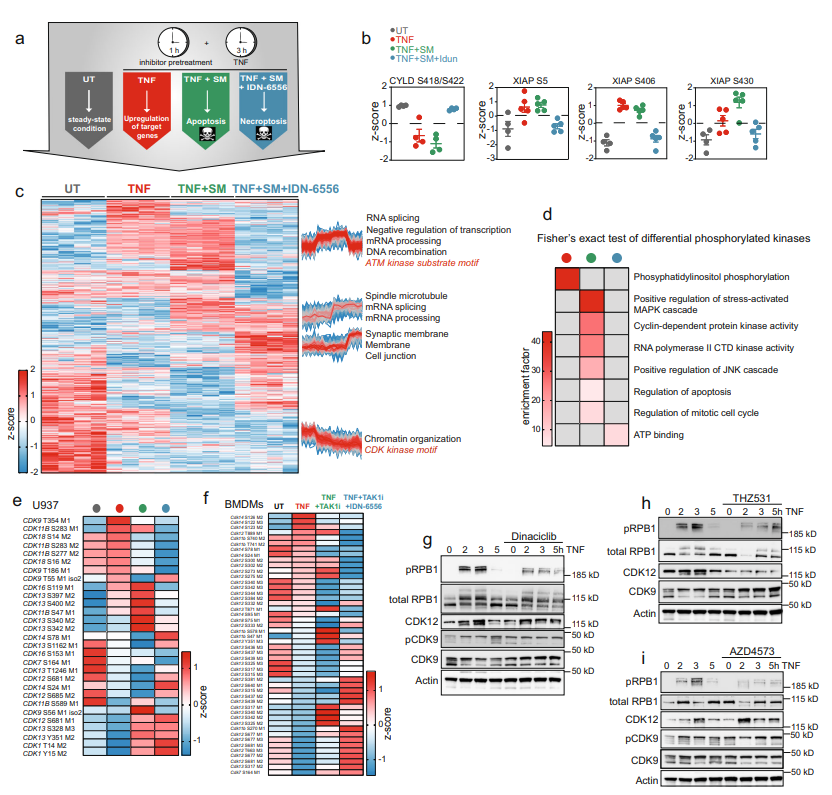
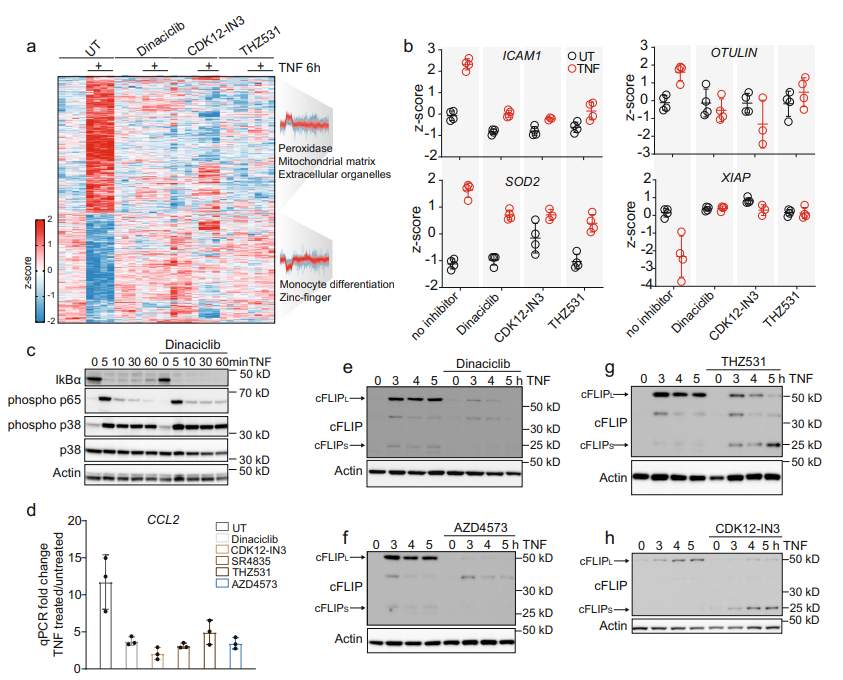
图5 CDK9和CDK12/13抑制剂影响TNF靶基因的转录
本研究通过DIA磷酸化蛋白质组学与亚细胞定位和激酶抑制剂分析相结合,深入分析了TNF受体下游的信号事件,阐明了数千个磷酸化事件的动力学、激酶底物关系和定位变化,提示了针对不同转录的CDKs的抑制剂可以作为抗炎剂或肿瘤细胞杀伤剂,深入全面的磷酸化水平的数据为后续研究提供了宝贵资源。

Nat Commun(IF 14.9)| 组学领军大牛Matthias Mann利用DIA磷酸化组深度剖析促炎信号通路
作者:上海中科新生命生物科技有限公司 2021-12-30T18:51 (访问量:2021)
上海中科新生命生物科技有限公司 商家主页
地 址: 上海市园美路58号1号楼15-18楼
联系人: 徐
电 话: 021-54665263
传 真:
Email:marketing@aptbiotech.com
相关咨询
会议邀请 | 第8届全国植物蛋白质研究大会暨首届贵阳生命科学新高地科学家论坛 (2023-07-07T14:37 浏览数:13906)
项目文章Cell(IF 64.5)| 中国科技大学探索食物过敏谜团 (2023-07-07T14:22 浏览数:14093)
Gastroenterology(IF 29.4)| 基于机器学习算法开发的外泌体miRNA生物标志物用于胰腺导管腺癌早期诊断 (2023-07-05T15:54 浏览数:11701)
Cancer Letters(IF 9.7)|天津市环湖医院利用Labelfree揭示超声-替莫唑胺联合诱导胶质瘤细胞的凋亡机制 (2023-06-30T09:37 浏览数:12754)
Excel表免费下载 | 速来围观!2023年影响因子发布 (2023-06-29T09:35 浏览数:11456)
外泌体多组学创新解决方案,精准、前沿的疾病诊断生物标志物 (2023-06-28T10:20 浏览数:15697)
Immunity (IF=43.474)丨单细胞+空间联合揭示肉芽肿形成的异常淋巴发育进程 (2023-06-26T17:28 浏览数:11849)
专家齐聚 亮点回顾 | 2023年海口·中医药创新多组学研究论坛圆满落幕 (2023-06-25T10:10 浏览数:16442)
项目文章Plant J(IF 7)| 杭州师范大学王慧中团队通过空间代谢+单细胞测序等揭示红豆杉幼茎细胞特异的紫杉烷合成调控模式 (2023-06-25T09:42 浏览数:13984)
项目文章Gut Microbes(IF 9.434)| 肠道微生物竟是导致胆囊切除术后患者腹泻的元凶? (2023-06-14T16:35 浏览数:11392)
